荧光定量PCR
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|---|---|---|---|
| YM2039 | 统计学分析 | /基因/图 | 50 | |
| YM2020 | miRNA qPCR检测 | /基因/样 | 100 | |
| YM2013 | miRNA引物合成 | 1 OD | 120 | |
| YM2051 | TaqMan探针引物合成 | 1 OD | 1500 | |
| YM2055 | 标准曲线(qPCR) | /基因 | 300 | |
| YM2015 | RNA电泳 | 板(8个样) | 300 | |
| Y3363-100 | Universal Blue Multiplex Probe One-Step RT-qPCR Kit | 100 rxns | 700 | |
| Y6078-100 | 荧光定量PCR封板膜(高粘性) | 100张/盒 | 200 | |
| Y6080-100 | 荧光定量PCR封板膜(压敏高粘plus型) | 100张/盒 | 1000 | |
| YMP-2 | 微孔板离心机(PCR反应板专用型) | 台 | 2000 | |
| YS-E30 | 封膜仪(便捷型) | 台 | 9000 | |
| YS-A20 | 封膜仪(智能型) | 台 | 12000 |
此处以 G3328 通用型彩色示踪染料法SYBR Green qPCR预混液(2×,含UDG) 为例
推荐qPCR反应体系:
Component | 20 μL rxn | 50 μL rxn | Final Concentration |
2×Universal Blue SYBR Green qPCR Master Mix (with UDG) | 10 μL | 25 μL | 1× |
Forward Primer (10 μM)a | 0.4 μL | 1 μL | 0.2 μM |
Reverse Primer (10 μM)a | 0.4 μL | 1 μL | 0.2 μM |
Templateb | Variable | Variable | as required |
Nuclease-free Water | Add to 20 μL | Add to 50 μL |
a.通常引物终浓度为0.2 μM可以得到较好扩增效果。反应性能较差时,可以在0.2-1.0 μM范围内调整引物浓度。
b.模板添加量因模板溶液中存在的靶基因的拷贝数不同而不同,进行梯度稀释研讨适当的模板添加量。在20 μL反应体系中模板DNA添加量最好在100 ng以下。以RT-PCR反应的cDNA(RT反应液)为模板时,添加量不要超过PCR反应液总体积的10%。
PCR反应程序(可根据机型适当调整):
A. 两步法 | B. 三步法 | ||||||||
阶段 | 步骤 | 循环数 | 温度 | 时间 | 阶段 | 步骤 | 循环数 | 温度 | 时间 |
Stage 1 | UDG孵育 | 1 | 50℃ | 2 min | Stage 1 | UDG孵育 | 1 | 50℃ | 2 min |
Stage 2 | 预变性 | 1 | 95℃ | 30 sec | Stage 2 | 预变性 | 1 | 95℃ | 30 sec |
Stage 3 | 变性 | 40 | 95℃ | 15 sec | Stage 3 | 变性 | 40 | 95℃ | 15 sec |
退火/延伸 | 60℃ | 30 seca | 退火 | 55-65℃ | 10 sec | ||||
延伸 | 72℃ | 30 seca | |||||||
Stage 4 | 熔解曲线 | 1 | 仪器默认设置 | Stage 4 | 熔解曲线 | 1 | 仪器默认设置 | ||
a.若需提高扩增特异性,可使用两步法程序或提高退火温度;若需提高扩增效率,可使用三步法程序或延长延伸时间。

(1)熔解曲线双峰:
a.杂峰在主峰之前,即代表有引物二聚体的存在,此种情况可尝试重新设计引物;
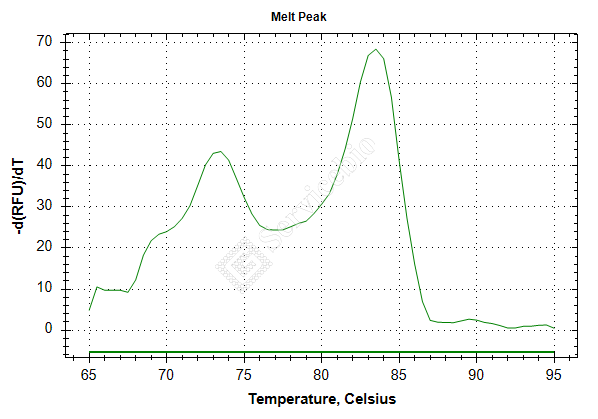
b.杂峰在主峰之后,大多由非特异性扩增引起,可尝试调整稀释倍数、减少引物等来进行调整;
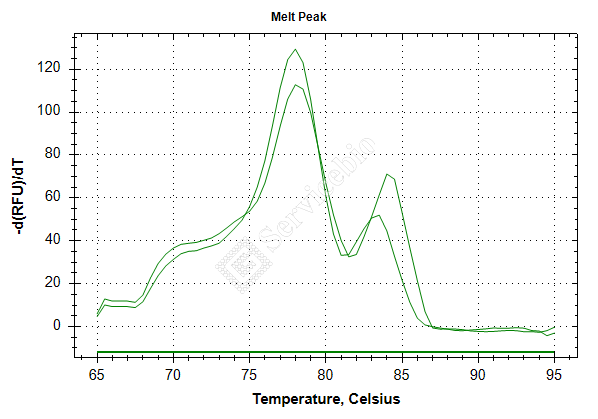
(2)一般Ct值在15-30之间,表达量太低或太高说明实验结果参考价值不大:
a.Ct值过大:
现象 | 原因 | 解决方案 |
Ct值过大 | 1.PCR产物太长 | 重新设计引物,长度建议100-200bp |
2.扩增效率低 | a.引物不能有效退火,重新设计引物;b.充分混匀试剂,规范操作减少移液误差;c.反应程序不合适,更改程序 | |
3.基因丰度较低 | 采用更灵敏的方法进行检测,增加模板量 | |
4.反应成分降解或模板量偏低 | a.检查RNA质量;b.提高反转录的效率 |
b.Ct值过小:
现象 | 原因 | 解决方案 |
Ct值过小 | 1.模板浓度高 | 更高比例的稀释cDNA,减少模板RNA用量 |
2.NTC和NRC存在污染 | 更换试剂,或含UDG试剂,可防止污染试剂 | |
3.引物设计不合适 | 优化程序,避免非特性扩增 |
c.无Ct值或无信号:
现象 | 原因 | 解决方案 |
无Ct值或无信号 | 1.循环数不够 | 建议扩增循环数35以上,可根据实际情况增加循环数至45 |
2.引物或探针降解 | 探针退火温度偏低,进行凝胶电泳实验,检测是否存在扩增产物 | |
3.模板上样不足或降解 | a.检测RNA质量;b.提高反转录的效率;c.避免cDNA反复冻融 |
(3)标准曲线关系不佳:
现象 | 原因 | 解决方案 |
标准曲线线性关系不佳 | 1.加样误差 | a.规范操作,减少移液误差;b.引物或者模板预混后再分别点样 |
2.标准品降解 | 改变稀释精度,增加稀释梯度 | |
3.模板存在抑制物或浓度过高 | a.避免cDNA反复冻融;b.重新制备稀释标准品 | |
4.引物或探针不佳 | 重新设计引物和探针 | |
5.PCR酶灵敏度低 | 更换灵敏度更高的试剂 |
