PCR技术
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|---|---|---|---|
| YM2017 | 普通PCR | /基因/样 | 50 | |
| YM2029 | 测序(一代测序) | 反应 | 18 | |
| YT-9600 | PCR仪 | 台 | 28000 | |
| YGQ-08 | PCR-8联管压/起盖器 | 个 | 150 |
实验原理
PCR技术,又叫聚合酶链反应(polymerase chain reaction,PCR),在体外模拟体内DNA复制的过程。PCR反应过程中,在DNA聚合酶的作用下,以母链DNA为模板,在体系中加入dNTP、引物、Mg2+等,以引物为延伸起点,经过变性、复性、延伸等步骤,进行半保留复制得到与母链互补的DNA的过程,从而快速得到任意DNA目的片段。

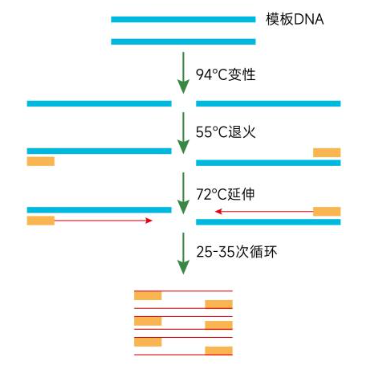
操作步骤
以G3304-01 2×Fast sTaq PCR预混液为例
推荐PCR反应体系:
| Component | 20 μL rxn | 50 μL rxn | Final Concentration |
| Templatea | Variable | Variable | as required |
| Forward Primer (10 μM)b | 0.8 μL | 2 μL | 0.4 μM |
| Reverse Primer (10 μM)b | 0.8 μL | 2 μL | 0.4 μM |
| 2×Fast sTaq PCR Master Mix | 10 μL | 25 μL | 1× |
| (DMSO, optional)c | (0.6 μL) | (1.5 μL) | (3%) |
| ddH2O | Add to 20 μL | Add to 50 μL |
a:以质粒或噬菌体DNA为模板时,推荐添加量为50 ng-5 pg每50 μL体系;以基因组DNA为模板时,推荐添加量为250 ng-50 ng每50 μL体系;cDNA为模板时,推荐稀释2-100倍,添加量不超过总体积的10%;以菌液或粗提样本为模板时,添加量不超过反应体积的10%。过量的模板容易导致非特异扩增,过少的模板容易导致PCR扩增效率低。
b:引物终浓度使用范围0.2-1.0 μM,推荐引物浓度为0.4 μM,过少的引物可能会导致扩增产量低或无扩增,过量的引物可能会导致非特异扩增。
c:高GC模板可在反应体系中额外添加不超过10%的DMSO。
推荐PCR扩增条件:
| Step | Temperature | Time | Cycles |
| Initial Denaturationa | 95℃ | 30 s-120 s | 1 |
| Denaturation | 95℃ | 5-10 s | 25-35 |
| Annealingb | 50-72℃ | 10-30 s | |
| Extensionc | 72℃ | 5-15 s/kb | |
| Final extension | 72℃ | 5-10 min | 1 |
| Hold | 4℃ | Forever |
a:预变性时间30 s适用于大多数常规模板,复杂模板可延长变性时间至2 min。
b:对于复杂模板,含兼并引物的扩增,退火时间可延长至30 s。
c:质粒等简单模板推荐延伸速度5-10 s/kb;常规基因组模板推荐延伸速度10-15 s/kb;复杂模板15-30 s/kb。
不同PCR预混液 应用参数对比
| PCR 预混液 | ||||||||||||
| 特征 | 货号 | 产品 | 热启动 | 扩增长度 | 延伸速率 | 保真度与Taq比较 | 产物末端结构 | 产物末端结构 | 5'→3'外切酶活性 | 3'→5'外切酶活性 | 应用 | |
| 常规PCR | 普通PCR | G3302 | 2 x Taq PCR Master Mix | √ | ≤ 8 kb | 1 min/kb | 1 × | 3' A | 3' A | 有 | 无 | •菌落PCR•基因鉴定•高GC 模板 |
| 快速PCR | G3304 | 2 x Fast Taq PCR Master Mix | ≤ 10 kb | 5-15 s/kb | 1 × | 3' A | 3' A | 有 | 无 | •菌落PCR•基因鉴定•高GC 模板 | ||
| 高保真PCR | 高保真度 | G3305 | 2 x Fast Pfus PCR Master Mix | ≤ 12 kb | 5-15 s/kb | 10 × | 平末端 | 平末端 | 无 | 有 | •菌落PCR•基因鉴定•高GC 模板•克隆•定点突变•模板扩增用于测序 | |
| 超高保真度 | G3306 | 2 x Fast High Fidelity PCR Master Mix | ≤ 12 kb | 5-15 s/kb | 50 × | 平末端 | 平末端 | 无 | 有 | •菌落PCR•基因鉴定•高GC 模板•克隆•定点突变•模板扩增用于测序 | ||
| 直接扩增PCR | 动物组织直扩 | G3310 | Animal Tissue Direct PCR Kit | ≤3 kb | 10 s/kb | / | / | / | / | / | •基因鉴定 | |
| 小鼠基因分型直扩 | G3311 | Mouse Genotyping Kit | ≤ 2 kb | 10 s/kb | / | / | / | / | / | •基因鉴定 | ||
| 血液直扩 | G3312 | Blood Direct PCR Kit | ≤ 5 kb | 10 s/kb | / | / | / | / | •各种新鲜血液、抗凝血、血卡基因鉴定 | |||
| 植物直扩 | G3313 | Plant Direct Tissue PCR Kit | ≤2 kb | 10 s/kb | / | / | / | / | •基因鉴定 | |||
| 其他 | 长片段扩增 | G3307 | 2 x LA PCR Master Mix | ≤ 30 kb | 5-30 s/kb | 6 × | 3' A/平末端 | 3' A/平末端 | 有 | 有 | •长片段扩增 | |
| 亚硫酸氢盐转化后扩增 | G3346 | Taq U DNA polymerase(for bisulfife-treated DAN) | < 2 kb | 1 min/kb | 1 × | 3' A | 3' A | 有 | 无 | •扩增含有尿嘧啶的模板 | ||
| 问题 | 原因 | 解决方案 |
| 实验组无扩增条带 | 引物设计错误或降解 | 重新检查引物序列并设计合成引物 |
| 模板不纯、降解、模板量太低 | 1、提取核酸时,用新鲜取样的样本进行核酸的提取,注意环境中核酸酶污染,保证核酸提取的质量 2、避免模板反复冻融 3、使用抗逆性强、灵敏度高的DNA聚合酶 4、适当增加模板的量 | |
| 电泳体系问题 | 核酸染料是否加了、琼脂糖凝胶浓度是否正确、电泳缓冲液是否有问题 | |
| PCR扩增温度不正确 | 1、检查PCR扩增仪显示的温度是否与实际温度一致; 2、若变性温度过高,酶容易失活,温度过低,则变性不完全 | |
| PCR产物量少、条带亮度过低 | 引物量过少、引物设计不合理 | 1、增加引物用量; 2、重新设计引物,避免形成发夹结构或者二聚体 |
| DNA模板用量过少 | 可通过电泳检查模板浓度,适当增加DNA模板用量 | |
| DNA模板量过多 | DNA模板过多,会结合所有引物,抑制反应进行 | |
| DNA出现降解 | 清除核酸酶污染 | |
| PCR循环数不足 | 延长PCR循环数 | |
| 延伸时间不够 | 增加延伸时间 | |
| 变性时间过长 | 变性时间太长会导致DNA聚合酶失活 | |
| PCR产物出现多个条带 | 引物量偏大、引物不特异 | 1、减少引物用量; 2、重新设计特异的引物 |
| DNA模板用量过多 | 质粒用量应<50ng,基因组DNA用量应<200ng | |
| 有外源DNA污染 | 用核酸清除剂,保持操作台和实验器具的干净 | |
| PCR循环数过多 | 减少循环数 | |
| 退火温度过低,退火及延伸时间过长 | 减少延伸时间,优化退火温度 | |
| 酶质量不高 | 更换另一种酶 | |
| 反应液未充分反应 | 增加反应时间;也可更换PCR预混液,防止预混液本身的质量问题 | |
| 条带大小与目的条带不符 | 引物设计错误、选用错误 | 重新设计引物、选用正确的引物 |
| 模板使用错误 | 更换模板 | |
| 出现核酸污染 | 对实验仪器耗材、实验台,用核酸酶清除核酸污染 |
