
动物组织/细胞线粒体DNA提取试剂盒
- 50 T
动物组织/细胞线粒体DNA提取试剂盒,适用于分离完整度高的线粒体DNA,提取的动物组织或细胞线粒体DNA可用于YCR扩增, qYCR检测,测序等,搭配一科2×Fast sTaq YCR预混液(Y3315-01)+YCR仪 (YT-9600)进行YCR实验,实验结果更好。
产品信息
产品名称 | 产品编号 | 规格 |
动物组织/细胞线粒体DNA提取试剂盒 | Y3762-50T | 50T |
产品简介
线粒体DNA(mtDNA)是真核细胞生物第二套基因组DNA,是除细胞核之外唯一含有DNA的细胞器,并且具有很高的保守性,有独立于细胞核的蛋白翻译系统和遗传密码,这些特点使之成为很好的进化研究对象。
本产品提取的动物组织或细胞线粒体DNA可用于所有下游应用。
应用:
1. YCR扩增(如:人源线粒体指标有ND1、ATP8、COX1、CYTB、16S等)
2. qYCR检测
3. 测序
特点:
1. 采用碱裂解法分离完整度较高的线粒体DNA
2. 可减少核基因组DNA污染
3. 试剂包含指示剂,通过其颜色的变化,指示线粒体是否完全裂解
4. 纯化的线粒体DNA应用范围广
样本种类、样本量:
60-100 mg动物组织,1-2×107培养细胞
储存与运输
线粒体分离试剂A、线粒体分离试剂B、BSA Solution、RNase A冰袋(wet ice)运输,-20℃保存;其余试剂室温运输,室温储存;有效期12个月。
组成
Component Number | Component | Y3762-50T |
Y3762-1 | 线粒体分离试剂A | 100 mL |
Y3762-2 | 线粒体分离试剂B | 50 mL |
Y3762-3 | BSA Solution | 1 mL |
Y3762-4 | Buffer M1 | 15 mL |
Y3762-5 | Buffer M2 | 15 mL |
Y3762-6 | Buffer M3 | 20 mL |
Y3762-7 | Buffer YW | 10 mL(使用前加入40 mL无水乙醇) |
Y3762-8 | Elution Buffer | 6 mL |
Y3762-9 | RNase A | 150 μL |
Y3762-10 | Bind DNA Mini Columns (with Collection Tubes) | 50套 |
说明书 | 1份 | |
使用前准备
1. 提前预冷离心机至4℃。
2. 自备玻璃匀浆器,使用前冰上预冷。
3. Buffer M1在使用前先加入全部的RNase A并混匀,置于2-8℃保存。
4. 使用前请先检查Buffer M2是否出现混浊,如有混浊现象,可在37℃水浴中加热数分钟,即可恢复澄清。
5. Buffer M2使用后应立即拧紧盖子,避免试剂长时间与空气接触。
6. 使用前向Buffer YW加入40 mL无水乙醇。
操作流程图
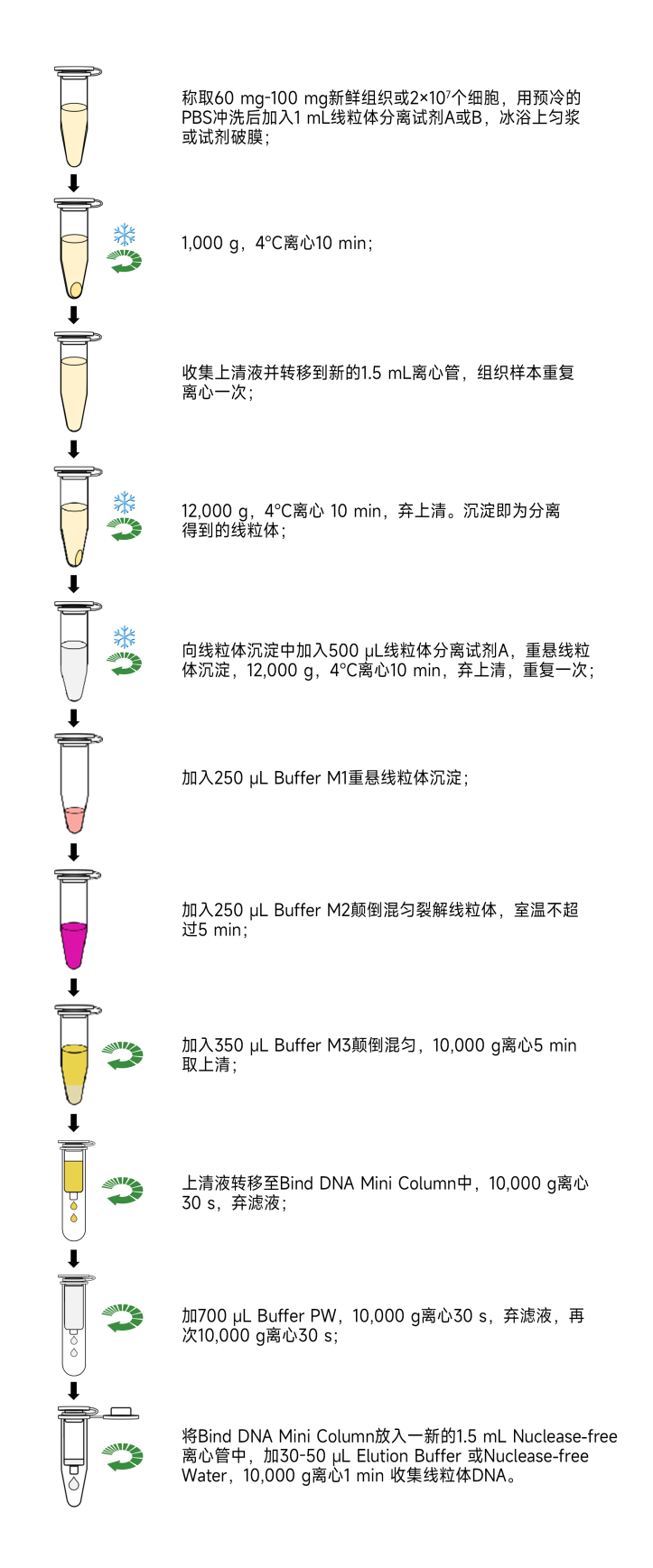
操作步骤
一、线粒体分离
组织或细胞匀浆:
1. 样本处理:
1) 组织匀浆:称取60-100 mg新鲜组织如肝脏、脑、心肌等,尽量去除脂肪组织和结缔组织等非目的组织,用1 mL预冷的PBS或生理盐水冲洗2次,用剪刀剪至1-3 mm3的碎块后加入1 mL预冷的PBS或生理盐水,1,000 g,4℃离心3 min,用移液器吸除上清;
2) 培养细胞匀浆:收集1-2×107个细胞,加入1 mL预冷的PBS,1,000 g,4℃离心5 min,弃上清,重复一次。
2. 加入1 mL线粒体分离试剂A(肌肉样本需加入20 µL的BSA Solution),使用移液器轻轻吹打重悬样本;
3. 将样品转移到预冷的小容量玻璃匀浆器中,冰浴上下研磨10-30次(细胞样本研磨次数为25-50次);
4. 将匀浆液转移到1.5 mL离心管中,1,000 g,4℃离心10 min(此时的沉淀包含细胞核、细胞碎片、未破碎的细胞等);
5. 对于组织样品,将上清转移至新的1.5 mL离心管,1,000 g,4℃再次离心10 min,细胞样本可直接进行下一步;
6. 将上清转移至新的1.5 mL离心管中,12,000 g,4℃离心10 min,弃上清,沉淀即为线粒体(如果后续需要对胞质蛋白进行分析,保存此步上清液);
7. 向线粒体沉淀中加入500 µL线粒体分离试剂A,使用移液器轻轻吹打重悬线粒体沉淀,12,000 g,4℃离心10 min,尽可能除去上清;
8. 重复步骤7;
9. 线粒体沉淀立即进行线粒体DNA提取或-80℃保存。
培养细胞试剂法裂解:
1. 收集1-2×107个细胞,加入1 mL预冷的PBS,1,000 g,4℃离心5 min,弃上清,重复一次;
2. 加入1 mL预冷的线粒体分离试剂B,使用移液器轻轻反复吹打25-50次,冰上孵育10 min;
3. 1,000 g,4℃离心10 min(此时的沉淀包含细胞核、细胞碎片、未破碎的细胞等,请勿丢弃,进行二次破膜);
4. 将上清转移至新的1.5 mL离心管中,12,000 g,4℃离心10 min,弃上清,沉淀即为线粒体(如果后续需要对胞质蛋白进行分析,保存此步上清液);
5. 将步骤3得到的沉淀重复步骤2-4操作进行二次破膜收集线粒体沉淀;
6. 向两管线粒体沉淀中各加入250 µL线粒体分离试剂A,使用移液器轻轻地重悬线粒体沉淀并合并为一管,12,000 g,4℃离心10 min,弃上清;
7. 加入500 µL线粒体分离试剂A,12,000 g,4℃离心10 min,弃上清;
8. 线粒体沉淀立即进行线粒体DNA提取或-80℃保存。
二、线粒体DNA提取
1. 向60-100 mg动物组织或1-2×107个培养细胞分离的线粒体沉淀中加入250 μL Buffer M1,使用移液器吹打混匀,此时溶液为红色;
2. 向离心管中加入250 μL Buffer M2,温和地上下翻转6-8次使线粒体充分裂解(溶液颜色为澄清的紫色;如紫色中混杂有浑浊的红色,则说明裂解不充分,继续混匀直至溶液颜色完全变为澄清的紫色,此步最好不超过5 min);
3. 向离心管中加入350 μL Buffer M3,立即快速地上下颠倒混匀6-8次,充分混匀,此时将出现絮状沉淀,10,000 g离心5 min(溶液为澄清的黄色,如在黄色中混有紫色,则说明复性不充分,继续混匀至溶液颜色完全变为澄清的黄色);
4. 将上清液转移至Bind DNA Mini Column中,注意尽量不要吸取沉淀,10,000 g离心30 s,弃去Collection Tube中的废液,将Bind DNA Mini Column放入Collection Tube中;
5. 向Bind DNA Mini Column中加入700 μL Buffer YW(使用前请先检查是否已加入无水乙醇),10,000 g离心30 s,弃掉废液;
6. 将Bind DNA Mini Column放入Collection Tube中,10,000 g离心30 s,除去残留的液体;
7. 将Bind DNA Mini Column放入一新的1.5 mL Nuclease-free离心管中,向Bind DNA Mini Column的膜中间位置悬空滴加30-50 μL Elution Buffer或Nuclease-free Water(60-65℃预热Elution Buffer或Nuclease-free Water后再使用效果更好),10,000 g离心1 min,收集线粒体DNA溶液(注意:为了提高线粒体DNA的回收量,可将离心得到的溶液重新加回Bind DNA Mini Column中,10,000 g离心1 min,收集线粒体DNA溶液)。
注意事项
1. 请勿使用冻存组织或细胞。
2. 分离线粒体的所有步骤需在冰上进行,所用溶液及器具需提前预冷。
3. 肌肉或心脏组织分离线粒体时可适当增加研磨次数。
4. 培养细胞试剂法分离线粒体可以进行高通量操作,线粒体得率可能低于匀浆法。
5. 如果处理大于100 mg组织或2×107个细胞,需按比例增加各试剂用量。
6. 线粒体DNA含量很低,电泳检测不到。
7. 各溶液使用后请及时将盖子拧紧,防止溶剂挥发。
8. 操作时请穿实验服,并佩戴一次性手套。
产品仅供科研用途,不用于临床诊断!
实验案例
使用Y3762 动物组织/细胞线粒体DNA提取试剂盒的试剂裂解法提取1×107 293FT细胞线粒体DNA,进行qYCR扩增13个线粒体编码基因以及2个线粒体rRNA基因,结果显示(图1):15个线粒体特异都能有效扩增,线粒体DNA提取效果较好。
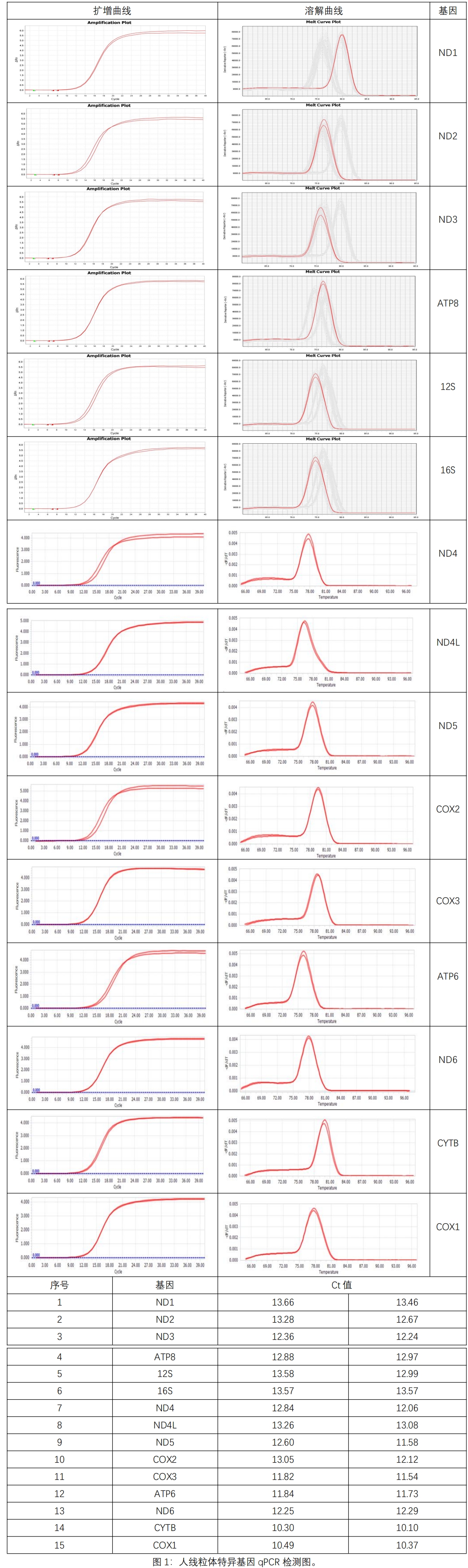
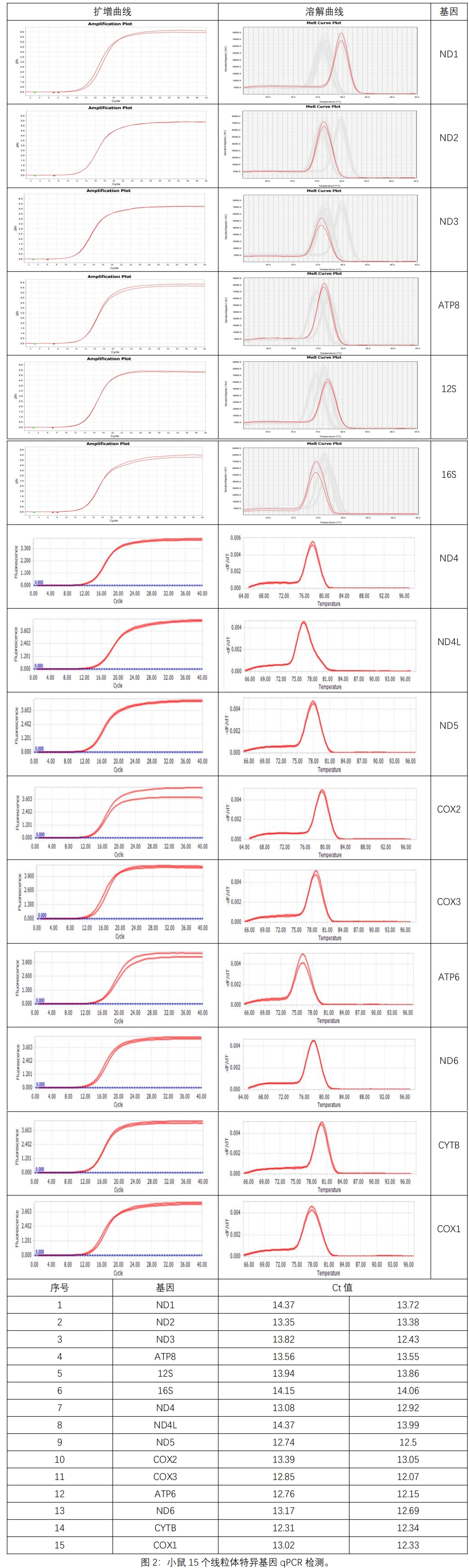
2. 使用Y3762 动物组织/细胞线粒体DNA提取试剂盒提取100 mg小鼠肌肉组织线粒体DNA,进行qYCR扩增13个线粒体编码基因以及2个线粒体rRNA基因,结果显示(图2):15个线粒体特异基因都能有效扩增,线粒体DNA提取效果较好。
(产品包装升级中,以实物为准。)
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|





