
抗体纯化试剂盒(Protein A琼脂糖凝胶法)
- 10 T
产品信息
| 产品名称 | 产品编号 | 规格 |
| 抗体纯化试剂盒(Protein A琼脂糖凝胶法) | Y2257-10T | 10 T |
产品简介
SweAgarose Protein A是用于分离和纯化单克隆抗体、多克隆抗体或Fc-融合蛋白的通用性亲和层析介质,具体性能见产品信息表2。Protein A是一种发现于金黄色葡萄球菌(Staphylococcus aureus)的细胞壁表面蛋白;Protein G是C型或G型链球菌(Streptococcal bacteria)表达的免疫球蛋白结合蛋白;Protein A和Protein G功能相似,能特异性地与哺乳动物免疫球蛋白(Immunoglobulin,Ig结合;本产品使用的是基因改造后的Protein A,不仅能维持其本身的Ig亲和特性,同时也去除了天然蛋白本身的非主要结合域以降低非特异性结合,以高度交联的琼脂糖凝胶为基质,修饰的耐碱重组Protein A为配基,具有很高的物理化学稳定性。
抗体纯化试剂盒(Protein A琼脂糖凝胶法)提供了5 mL SweAgarose Protein A 填料、重力柱、抗体纯化所需的缓冲液,方便客户使用,操作简单,纯化效率高。试剂盒组分见表 3。
产品信息
| 指标名称 | 描述 |
| 产品内容 | 50%(v/v) 琼脂糖凝胶保存于特殊保存液中 |
| 凝胶类型 | 4%交联琼脂糖凝胶 |
| 偶联蛋白 | 耐碱重组Protein A |
| 偶联蛋白分子量 | ~25 kDa(Protein A) |
| 结合载量 | 10-20 mg/mL 凝胶 |
| 特异性 | 来自不同物种的抗体,包括小鼠、人源、大鼠、山羊、绵羊、牛 |
| 粒径范围(μm) | 30~150 μm |
| 平均粒径(μm) | 90 μm |
| 化学稳定范围 | 常用的水相缓冲液;500 mM NaOH ;6 M盐酸胍; 8 M尿素;70% 乙醇 |
储存与运输
冰袋(wet ice)运输;5×蛋白上样缓冲液(无气味、还原型)请保存于-20℃,其他2-8℃保存,有效期12个月。
试剂盒组成
| 货号 | 组成 | 规格 | 储存温度 |
| Y2217-5ML | SweAgarose Protein A | 5 mL | 2-8℃ |
| Y2257-1 | PBS, 10×(pH7.4) | 100 mL | 2-8℃ |
| Y2257-2 | 洗脱液(Acid Elution Buffer) | 2×75 mL | 2-8℃ |
| Y2257-3 | 中和液(Neulization Elution Buffer) | 15 mL | 2-8℃ |
| Y2086-1ML | 5×SDS-PAGE蛋白上样缓冲液(无气味、还原型) | 1 mL | -20℃ |
| Y6075-12 | 亲和层析柱空柱(12 mL) | 5套 | 常温 |
| 说明书 | 1份 | ||
操作步骤
1. 纯化试剂准备:
抗体纯化相关试剂配方参考如下,用户可根据具体实验情况自行调整:
| 组分 | 组分配方 |
| 平衡/洗杂液(1×PBS) | 1×PBS:137 mM NaCl,2.7 mM KCl, 10 mM Na2HPO4, 2.0 mM KH2PO4 |
| 洗脱液(Acid Elution Buffer) | 100 mM 甘氨酸, pH 2.8 |
| 中和液(Neulization Elution Buffer) | 1.0 M Tris-HCl, pH 9.0 |
注意:纯化前先配制1×PBS和1×蛋白上样缓冲液。
1×PBS的配制:将10×PBS缓冲液用超纯水稀释至1×,即为1×PBS;例如1 mL 10×PBS缓冲液加入9 mL超纯水,混匀后即为1×PBS缓冲液;
1×蛋白上样缓冲液(无气味、还原型)的配制:取适量5×蛋白上样缓冲液(还原型)用超纯水稀释5倍即为1×蛋白上样缓冲液(还原型);例如0.2 mL 5×蛋白上样缓冲液(还原型)加入0.8 mL超纯水,混匀后即为1×蛋白上样缓冲液(还原型)。
2. 层析重力柱组装及平衡处理:
重力柱组装:详细方法可参考本公司亲和层析柱空柱(货号Y6075-12)装柱流程。
筛板处理:用纯水或者填料保存液预先对筛板进行脱气处理,将下筛板推至空柱底部后加入适量保存液浸润底部,封住下出液口;
装填:将 SweAgarose Protein A 填料上下颠倒充分混匀后取适量加入层析柱(避免剧烈摇晃),室温静置10 min,待凝胶与溶液分层后,打开底部出液口让乙醇通过重力作用缓慢流出,同时将上筛板垂直推至填料表面,添加保存液至满柱,装柱完成;
平衡:向装填好的柱子中加入5 个柱体积的去离子水将乙醇冲洗干净后,再用5-8个柱体积的平衡液平衡柱子,平衡结束后即可上样。
注意:柱体积指填料体积;建议装填高度不超过空柱高度 1/3;填料保护液占比约50%请根据填料载量及蛋白表达量选取合适地体积的乙醇和填料混合液。
3. 样品制备
3.1 上柱之前要确保样品溶液有合适的离子强度和pH值,可以用平衡液对血清样品、腹水或细胞培养液稀释,或者样品用平衡液透析。
3.2 上柱之前样品建议离心或用0.22 μm或0.45 μm滤膜过滤,减少杂质,提高蛋白纯化效率和防止堵塞柱子。
4. 纯化流程
上样:将处理好的样品直接加入平衡好的柱子中,以加入的体积控制流速快慢,收集流出液,用于SDS-PAGE分析蛋白质的结合情况;
淋洗:使用2-5个柱体积的平衡液冲洗上样后的柱子,洗去部分杂蛋白;
洗杂:使用10-15个柱体积的洗杂液冲洗柱子,分管收集洗杂液,用于SDS-PAGE分析蛋白质的洗杂程度,也可用考马斯亮蓝G250(#Y2050)快速检测洗杂终点;
洗脱:使用约3-5个柱体积的洗脱液(Acid Elution Buffer)冲洗柱子,分管按体积收集洗脱液并立即用1/10体积中和液(Neulization Elution Buffer)中和到抗体稳定的pH,SDS-PAGE分析每管蛋白质洗脱情况;
柱再生:洗脱结束后,应立即用2~3个柱体积的洗脱缓冲液清洗介质,然后用2~3个柱体积的平衡液冲洗平衡。如工艺过程中的变性蛋白或脂质等物质,在再生过程中无法洗脱,可以通过在位清洗操作去除。
5. 在位清洗(CIP):
介质经过长期使用后,过多的污染物会使柱床反压增大,从而降低柱效与介质吸附载量,甚至损害介质的寿命。定期CIP可有效保护介质。如果介质轻微污染,可每1-5次循环进行一次CIP;但对于实验后污染严重的介质,建议每次使用之后都进行在位清洗,以保证结果的可重复性。
对于强结合蛋白、沉淀、强疏水性蛋白及脂类物质去除:
可用2 M NaCl 清洗2个柱体积,去除较强的非特异性结合蛋白;
可用100-500 mM NaOH 清洗柱子,接触时间10~15 min,立即用纯水冲洗3-4个柱体积,再用平衡液冲洗5个柱体积;
可用6 M盐酸胍冲洗2-3个柱体积,立即用平衡液清洗至少5个柱体积。
注意事项
1. 试剂盒中组分SweAgarose Protein A请勿保存于-20℃或反复冻融,否则会影响凝胶的性能,造成不必要的实验误差。
2. 凝胶需维持pH为6-8,避免高速离心、干燥或冻存,否则可能会引起凝胶聚团。
3. 凝胶使用前要充分混匀,混匀操作须轻柔,不宜剧烈涡旋震荡等,避免抗体变性等。
4. 本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
5. 为了您的安全与健康,请穿实验服并戴一次性手套操作。
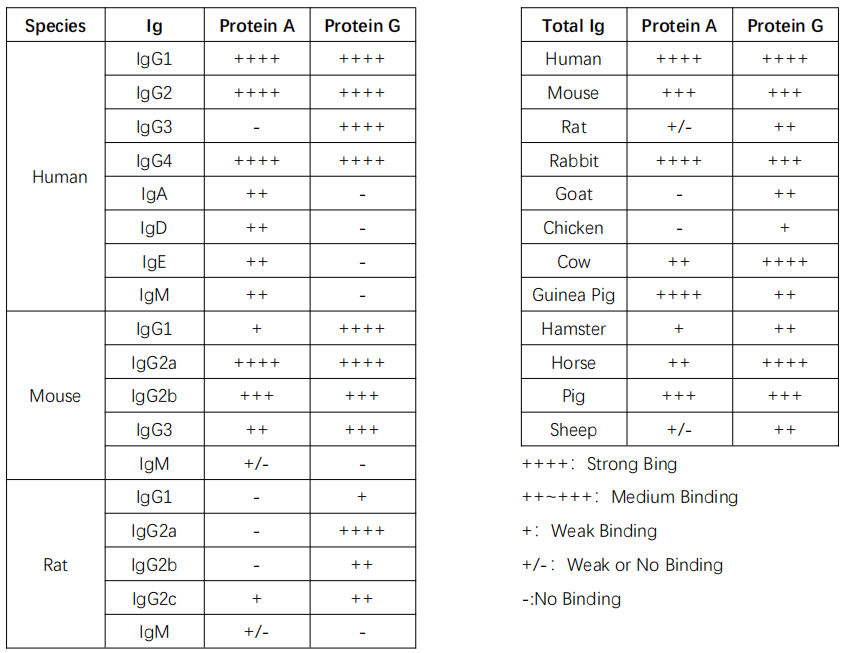
6. Protein A、Protein G对不同种属来源及亚型抗体结合能力见附表一。
附表一
产品仅供科研用途,不用于临床诊断!
(产品包装升级中,以实物为准。)
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|

